La presión atmosférica se refiere a la presión ejercida por el aire sobre la Tierra. Siendo así, es claro que afecta directamente ciertos fenómenos físicos. Pero es necesario destacar que de igual manera, la presión atmosférica en química puede incidir en el resultado de ciertos experimentos.


Entendamos la acción de la presión atmosférica
Si la superficie terrestre fuera enteramente plana, la presión atmosférica sería la misma en cualquier punto de ella. Pero no es así; ya que existen montañas, lomas, llanuras, etc. Por lo tanto cuando hay mayor altitud se genera menor presión atmosférica. Caso contrario cuando la altura es menor, incluso a nivel del mar, la presión es mucho mayor.
Estos datos sirven de marco para tener una idea de la intensidad o grado de presión atmosférica en ciertos puntos de la Tierra. Pero obtener datos exactos resulta muy complicado, especialmente porque la temperatura y la presión del aire varían constantemente.
Es posible obtener un pronóstico del tiempo
Si se logra medir la presión atmosférica en un sitio determinado, pocas conclusiones se pueden obtener de dicho dato.
La variación de esta presión determinada en un período de tiempo largo junto a datos meteorológicos como humedad, vientos, etc., determina el tiempo atmosférico del lugar analizado. Incluso permite realizar pronósticos del tiempo.
Vemos entonces una acción poco exacta de la presión atmosférica en fenómenos físicos. Sin embargo la presión atmosférica en química actúa con mayor nitidez y claridad.
Una forma fácil de visualizar la presión atmosférica en química
Realizar un simple experimento en casa puede ayudar a visualizar de mejor manera la acción de la presión atmosférica en química. Se requieren de materiales simples como una vela, algunas cerillas o mechero, un vaso de tubo, agua y un plato hondo.
Se vierte agua en el plato considerando un nivel en el que, al poner la vela encima, el líquido no apague la llama. Luego se coloca con mucho cuidado la vela en medio del plato y se enciende. Al notar que la llama se mantiene estable, entonces se cubre con el vaso.
Presencia de la presión atmosférica en el experimento
En el proceso de combustión de la cera de la vela actúa el oxígeno. Esta reacción química genera dióxido de carbono (CO2) y agua (H2O). Durante tal proceso de combustión el agua se torna en vapor, condensándose luego como gotas en las paredes del vaso.
Aquí disminuye el volumen.
No solo por el cambio de estado del agua. Sino también porque el dióxido de carbono se enfría cuando hace contacto con las paredes del vaso. Vemos entonces que el volumen dentro del vaso se aminora mientras la presión atmosférica opresión externa no varía.
Esta es mayor que la presión interna, empuja al agua y la hace subir, es cuando se igualan las presiones.

 ¿Cómo se puede regular la presión atmosférica?
¿Cómo se puede regular la presión atmosférica? Cómo afecta la presión atmosférica a la presión sanguínea
Cómo afecta la presión atmosférica a la presión sanguínea Qué es presión atmosférica en termodinámica
Qué es presión atmosférica en termodinámica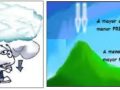 Qué es presión atmosférica en salud ocupacional
Qué es presión atmosférica en salud ocupacional Relación entre presión atmosférica y lluvia
Relación entre presión atmosférica y lluvia Relación entre presión atmosférica y temperatura
Relación entre presión atmosférica y temperatura Relación entre presión atmosférica y altura
Relación entre presión atmosférica y altura Imágenes sobre la presión atmosférica
Imágenes sobre la presión atmosférica